元素周期表填空
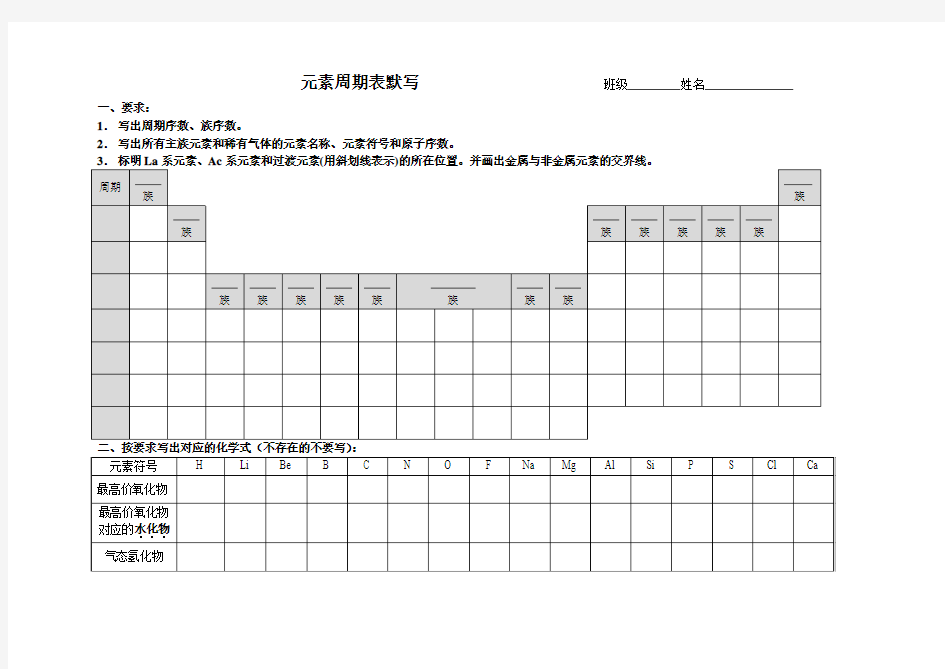
元素周期表默写班级姓名
一、要求:
1.写出周期序数、族序数。
2.写出所有主族元素和稀有气体的元素名称、元素符号和原子序数。
精 高中化学元素周期表知识点详解
第一节 元素周期表 一.元素周期表的结构 周期序数=核外电子层数主族序数=最外层电子数 原子序数 = 核电荷数 = 质子数=核外电子数 短周期(第1、2、3周期) 周期:7个(共七个横行) 周期表 长周期(第4、5、6、7周期)主族7个:ⅠA-ⅦA 族:16个(共18个纵行)副族 7个:IB-ⅦB 第Ⅷ族1个(3个纵行)零族(1个)稀有气体元素 【练习】 1.主族元素的次外层电子数(除氢) A .一定是8个 B .一定是2个 C .一定是18个 D .是2个、8个或18个2.若某ⅡB 族元素原子序数为 x ,那么原子序数为x+1的元素位于A .ⅢB 族B .ⅢA 族 C .ⅠB 族 D .ⅠA 族 3.已知A 元素原子的最外层电子数是次外层电子数的3倍,B 元素原子的次外层电子数是 最外层电子数的 2倍,则A 、B 元素 A .一定是第二周期元素 B .一定是同一主族元素 C .可能是二、三周期元素 D .可以相互化合形成化合物二.元素的性质和原子结构(一)碱金属元素: 1.原子结构 相似性:最外层电子数相同,都为 _______个 递变性:从上到下,随着核电核数的增大,电子层数增多 2.碱金属化学性质的相似性: 4Li + O 2 Li 2O 2Na + O 2 Na 2O 2 2 Na + 2H 2O =2NaOH + H 2↑ 2K + 2H 2O = 2KOH + H 2↑ 2R + 2 H 2O = 2 ROH + H 2 ↑产物中,碱金属元素的化合价都为+1价。结论:碱金属元素原子的最外层上都只有 _______个电子,因此,它们的化学性质 相似。 3.碱金属化学性质的递变性: 递变性:从上到下(从Li 到Cs ),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。所以从 Li 到Cs 的金属性逐渐增强。 结论:1)原子结构的递变性导致化学性质的递变性。2)金属性强弱的判断依据: 与水或酸反应越容易,金属性越强;最高价氧化物 对应的水化物(氢氧化物)碱性越强,金属性越强。4.碱金属物理性质的相似性和递变性: 1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有 展性。 2)递变性(从锂到铯):①密度逐渐增大( K 反常) ②熔点、沸点逐渐降低 点燃 点燃
2020高考化学元素周期表测试
第一章物质结构元素周期律 第一讲元素周期表 复习重点:元素周期表的结构;元素在元素周期表中的位置及其性质的递变规律。复习难点:元素在元素周期表中的位置及其性质的递变规律。 一、元素周期表的结构 把电子层数目相同各种元素, 按排成横行;再排成纵行得到一个表,这个表就叫元素周期表。元素周期表是的具体表现形式,它反映了相互联系的规律,是我们学习化学的重要工具。 1.周期:(1)周期序数= 电子层数,共个周期(、、短周期;、、 长周期;不完全周期)。填表: 类别周期序数起止元素包括元素种数核外电子层数 短周期 长周期 不完全周期 (2) 总称镧系元素。,总称锕系元素。在锕系元素中以后的各种元素,多数是人工进行核反应制得的元素,这些元素又叫做超铀元素。 2.族:(1)由构成的族,叫做主族;构成的族,叫做副族。(2)元素周期表的中部从族到族10个纵行,包括了族和全部副族元素,共六十多种元素,通称为过渡元素。因为这些元素都是,所以又把它们叫做过渡金属。(3)主族元素的族序数=元素原子的最外层电子数。周期表共18个纵行(个主族;个副族;一个族;一个族(、、三个纵行))。 二、元素性质与原子结构 (一)碱金属元素 元素名称核电荷数原子结构示意图最外层电子数电子层数 碱 金 属 元 素 个。单质密度逐渐,熔沸点逐渐。
2、碱金属的化学性质:钾的保存及取用方法: 。 (1)与氧气反应差异性: Li+O 2_(_色、氧化锂);_Na+O 2__(_色、过氧化钠);_K+O 2_(_色,_氧化钾);_Rb+_O 2 _(棕色、_氧化铷);_C S +_O 2 _(_色、_氧化铯)。 (2)与水反应差异性:(填反应现象) 2Li+2H 2O=2LiOH+H 2↑(__);2Na+2H 2O=2NaOH+H 2↑(剧烈);2K+2H 2O=2KOH+H 2↑(____、__);2Rb+2H 2O=2RbOH+H 2↑(更猛烈、燃烧、爆炸)。 (3)写出下列反应的化学方程式: 过氧化钾与CO 2: ;超氧化钾与水、CO 2: 、 ; 氧化锂与水、CO 2 : 、 。 (二)卤族元素 1、卤素原子结构(1)示意图:F Cl Br I 。 最外层电子数相同,但电子层数逐渐增大,得电子能力 ,非金属性 。 2、卤族元素单质的物理性质的变化规律 (随原子序数的递增) (1)颜色:__色~__色~___色~__色 (颜色逐渐加深 ) (2)状态: _态~_态~_态(3)熔沸点:逐渐__ (4)密度: 逐渐__ (5)水溶解性:逐渐__。 3、卤素单质与氢气反应 名称 反应条件 方程式 生成氢化物的稳定性 F 2 _____ H 2+F 2====2HF HF 很稳定 Cl 2 _____ H 2+Cl 2=====2HCl HCl 稳定 Br 2 _____ H 2+Br 2======2HBr HBr 较不稳定 I 2 _____ H 2+I 2======2HI HI ___稳定 2氯化钠水溶液反应:____________。 疑难点拨 一、元素周期表终点之迷 1869年2月,俄国化学家门捷列夫将当时已发现的63种元素列成元素周期表,并留下一些空格,预示着这些元素的性质。在元素周期表的指导下,人们“按因索骥”找出了这些元素。 元素种类到底是否有限? 周期表有否终点? 这是科学家们,也是诸位读者所关心的问题。 本世纪30~40年代,人们发现了92号元素,就有人提出92号是否是周期表的最后一种元素。然后从1937年起,人们用人工合成法在近50年时间又合成近20种元素,元素周期尾巴越长了。这时又有人预言,105号元素该是周期表的尽头了,其理由是核电荷越来越大,核内质子数世越来越大,质子间的排斥力 将远远超过核子间作用力,导致它发生蜕变,然而不久,又陆续合成了106~109号元素。这些元素存在的时间很短,如107号元素半衰期只有2微秒,照此计算是否周期表到尽头了? 1969年起,理论物理学家从理论上探索“超重元素”存在的可能性,他们认为具有2,光 500℃
高一化学元素周期表知识精讲.doc
高一化学元素周期表 【本讲主要内容】 元素周期表 元素周期表中主族元素性质的递变规律、原子结构、元素性质及元素在周期表中位置三者的关系、元素周期表的结构及应用、元素的推断等。其中元素周期表的结构及应用是学习的重点。 【知识掌握】 【知识点精析】 二. 原子结构、元素性质及元素在周期表中位置三者的关系 主族序数 原子半径 1.同周期左右: 非金属性增强。 2.同主族上下: 化学性质相似, 但又有递变。 1. 原子结构与元素在周期表中的位置关系: (1)核外电子层数=周期数
(2)主族元素的最外层电子数=价电子数=主族序数=最高正价数 (3)质子数=原子序数=原子核外电子数=核电荷数 (4)负价绝对值=8-主族数(限ⅣA~ⅦA) (5)原子半径越大,失电子越易,还原性越强,金属性越强,形成的最高价氧化物的相应水化物碱性越强,其离子的氧化性越弱。 (6)原子半径越小,得电子越易,氧化性越强,非金属性越强,形成的气态氢化物越稳定,形成最高价氧化物的相应水化物酸性越强,其离子的还原性越弱。 2. 周期表与电子排布 (1)最外层电子数等于或大于3(小于8)的一定是主族元素。 (2)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素又可能是副族或零族元素氦。 (3)最外层电子数比次外层电子数多的元素一定位于第二周期。 (4)某元素阴离子最外层电子数与次外层相同,该元素位于第三周期。 (5)电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期。 3. 从元素周期表归纳元素化合价的规律 (1)主族元素的最高正价数等于主族序数,等于主族元素原子的最外层电子数,其中氟无正价。非金属元素除氢外,均不能形成简单阳离子,金属元素不能形成简单阴离子。 (2)主族元素的最高正价数与最低负价数的绝对值之和为8,绝对值之差为0、2、4、6的主族依次为ⅣA、ⅤA、ⅥA、ⅦA族。 (3)非金属元素的正价一般相差2,如氯元素正化合价有+7、+5、+3、+1等,某些金属也符合此规律,如锡元素正化合价有+4、+2价 (4)短周期正价变化随原子序数递增,同周期有一个+1到+7价的变化(ⅠA~ⅦA);长周期有两个+1到+7价的变化(ⅠA~ⅦB,ⅠB~ⅦA)。 三. 元素周期表的结构 1. 周期 元素周期表分7个周期,第一、二、三为短周期,元素种类依次为2、8、8;第四、五、六周期为长周期,元素种类依次为18,18,32;第七周期为不完全周期,目前有32种元素。 除第一周期外,每一周期的元素都是从碱金属开始,逐渐过渡到卤族元素,最后以稀有气体元素结束。 2. 族 元素周期表中有18个纵行,分为16个族,其中7个主族、7个副族,还有1个零族和1个第Ⅷ族。 过渡元素包括全部副族和第Ⅷ族,都是金属,又称过渡金属。 除短周期外;族序数从左到右的顺序为:ⅠA→ⅡA→ⅢB→…ⅦB→Ⅷ→ⅠB→ⅡB→ⅢA →…→ⅦA→0族,前后从1→8更迭两次。 金属、非金属的分界线
元素周期表与元素周期律知识点归纳完美版
元素周期表与元素周期律知识点归纳 1、元素周期表共有横行,个周期。其中短周期为、、。所含元素种类为、、。长周期包括、、。所含元素种类为、、。 第七周期为不完全周期,如果排满的话有种元素。 2元素周期表有个纵行个族。包括个主族,个副族,一个族,一个第Ⅷ族(包括个纵行)按从左到右的顺序把16个族排列 。过度元素共包括个纵行(第纵行到第纵行)。包括哪些族。过渡元素全为元素。又称为。 3、写出七个主族和0族元素的名称和元素符号 ⅠA族 ⅡA族 ⅢA族 ⅣA族 ⅤA族 ⅥA族 ⅦA族 0族 4.同一周期第ⅡA族和第ⅢA族原子序数之间的关系 若元素位于第二、三周期,第ⅡA族的原子序数为a,则第ⅢA族的原子序数为 若元素位于第四、五周期,第ⅡA族的原子序数为a,则第ⅢA族的原子序数为 若元素位于第六周期,第ⅡA族的原子序数为a,则第ⅢA族的原子序数为 5、同一主族上下相邻两个周期原子序数之间的关系 若A在B的上一周期,设A的原子序数为a ⑴若A、B位于第ⅠA族或ⅡA族(过度元素的左边)则B的原子序数为。 ⑵若A、B位于第ⅢA族——ⅦA族(过度元素的右边)则B的原子序数为。 。 6、微粒半径大小判断的方法 。 。 。 7 与He原子电子层结构相同的简单离子。 与Ne原子电子层结构相同的简单离子。 与Ar原子电子层结构相同的简单离子。 阳离子与周期稀有气体原子的电子层结构相同。阴离子与周期稀有气体原子的电子层结构相同。 8、阴上阳下规律 9原子得电子能力强弱判断的方法 ⑴、原子得电子能力越强——单质的氧化性——元素的非金属性——阴离子的还原性——单
质与氢气化和的能力——生成的气态氢化物越——最高价氧化物对应水化物的酸性。 ⑵、另外可以通过单质间的置换反应判断得电子能力的强弱 如Cl2+Na2S=2NaCl+S得电子能力ClS 10、原子失电子能力强弱判断的方法 ⑴、原子失电子能力越强——单质的还原性——元素的金属性——阳离子的氧化性——单质与水或酸反应置换出氢的能力——最高价氧化物对应水化物的碱性。 ⑵、另外可以通过单质间的置换反应判断失电子能力的强弱 如Fe+CuSO4=FeSO4+Cu失电子能力FeCu 11、同一主族元素及其化合物性质的递变性: 同主族元素的原子,最外层电子数,决定同主族元素具有的化学性质。从上到下原子的核电荷数依次,原子的电子层数依次,原了半径逐渐;原子失电子能力逐渐,元素的金属性逐渐,单质的还原性逐渐,对应阳粒子的氧化性逐渐,单质与水或酸反应置换出氢气的能力逐渐,最高价氧化物对应水化物的碱性逐渐;原子得电子能力逐渐,元素的非金属性逐渐,单质的氧化性逐渐,对应阴离子的还原逐渐,单质与氢气化合的能力逐渐,最高价氧化物对应水化物的酸性逐渐。气态氢化物的稳定性逐渐。 12、同一周期元素及其化合物性质的递变性: 在同一周期中,各元素原子的核外电子层数,但从左到右核电荷数依次,最外层电子数依次,原子半径逐渐(稀有气体元素除外)。原子失电子能力逐渐,元素的金属性逐渐,单质的还原性逐渐,对应阳粒子的氧化性逐渐,单质与水或酸反应置换出氢气的能力逐渐,最高价氧化物对应水化物的碱性逐渐。 原子得电子能力逐渐,元素的非金属性逐渐,单质的氧化性逐渐,对应阴离子的还原逐渐,单质与氢气化合的能力逐渐,最高价氧化物对应水化物的酸性逐渐,气态氢化物的稳定性逐渐。 1.位、构、性的关系 根据原子结构、元素周期表的知识及相关条件可推算原子序数,判断元素在周期表中的位置等。 2.周期表中数字与性质的关系 (1)由原子序数确定元素位置的规律:只要记住稀有气体元素的原子序数就可以确定主族元素的位置。 He:2、Ne:10、Ar:18、Kr:36、Xe:54、Rn:86 ①若比相应的稀有气体元素的原子序数多1或2,则应处在下一周期的ⅠA或ⅡA,如88号元素,88-86=2,则应在第7周期第ⅡA。 ②若比相应的稀有气体元素的原子序数少1~5时,则应在第ⅦA~ⅢA,如84号元素在第6周
元素周期表45分钟测试
元素周期表45分钟测试 每题有一项或两项正确 1.下列各组微粒具有相同的质子数和电子数的是 A.OH-、H2O、F-B.NH3、NH4+、NH2- C.H3O+、NH4+、NH2-D.HCl、F2、H2S 2.已知元素X、Y的核电荷数分别是a和b,且它们的离子X m+和Y n-的核外电子排布相同,则下列关系式中正确的是 A.a=b+m+n B.a=b-m+n C.a=b+m-n D.a=b-m-n 3.下列金属中,按照金属性从弱到强的顺序排列的是 A.铝、镁、钠、钾B.镁、铝、钾、钠 C.钙、钾、铷、铯D.钙、钾、钠、锂 4.元素周期表中某ⅠA族元素原子序数为x,则同一周期的ⅢA族元素原子序数不可能为A.x+25 B.x+2 C.x+12 D.x+26 5.某元素X的核外电子数等于核内中子数。取该元素单质2.8 g与氧气充分作用,可得到6 g化合物XO2。该元素在周期表中的位置是 A.第三周期B.第二周期C.第ⅣA主族D.第ⅤA主族 6.钾的金属活动性比钠强,根本原因是 A.钾的密度比钠小 B.钾原子的电子层比钠原子多一层 C.钾与水反应比钠与水反应更剧烈 D.加热时,钾比钠更易汽化 7.碱金属钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列对其性质的预言中,错误的是A.在碱金属元素中它具有最大的原子半径 B.它的氢氧化物化学式为FrOH,是一种极强的碱 C.钫在空气中燃烧时,只生成化学式为Fr2O的氧化物 D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸 8.砹(At)是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是 A.砹的非金属性在卤素中是最弱的,At-易被氧化 B.砹化氢很稳定不易分解 C.砹化银不溶于水或稀HNO3 D.砹在常温下是白色固体 9.周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者4倍的是( ) A.电子数B.最外层电子数C.电子层数D.次外层电子数 10.某元素原子的最外电子层上只有2个电子,下列说法正确的是…………………( ) A该元素一定是金属元素B.该元素可能是非金屑元素 C该元素可能是第ⅡA族元素D.该元素一定是稀有气体元素 11.按Li、Na、K、Rb、Cs顺序递增的性质是…………………………………………( ) A.单质的还原性B.阳离子的氧化性C.原子半径D.单质的熔点 12.下列叙述正确的是( ) A.在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物 B.由于钠、钾的密度都小于1,所以,碱金属单质的密度都小于1 C.金属锂不能保存于煤油中,金属钾可以保存于煤油中 D.虽然自然界含钾的物质均易溶于水,但土壤中钾含量太少,故需施用钾肥 13、(镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质描述不正确的是() A在化合物中呈+2价 B 单质能与水反应放出氢气 C 镭比钙的金属性弱 D 碳酸镭难溶于水 14.科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IV A 族,称为类铅。关于它的性质,预测错误的是() A.它的最外层电子数为4 B.它的金属性比铅强 C.它具有+2、+3、+4价 D.它的最高价氧化物的水化物是强酸 15.在IIA族中,Be是惟一可以生成含氧酸根(铍酸根离子:BeO)的元素,与铍的性质相似的短周期元素是()A.Na B.Mg C.Al D.Si
高中元素周期表知识点
高中元素周期表知识点 高中元素周期表知识点 元素周期表共分18纵行: 其中 第1、2、13、14、15、16、17七个纵行依次为ⅠA族、ⅡA族、ⅢA族、ⅣA族、ⅤA族、ⅥA族、ⅦA族(纵行序号的'个位数与主族序数相等); 第3、4、5、6、7、11、12七个纵行依次为ⅢB族、ⅣB族、ⅤB 族、ⅥB族、ⅦB族、ⅠB族、ⅡB族(纵行序号个位数与副族序数相等); 第8、9、10三个纵行为合称为Ⅷ族;第18纵行称为0族。 ⅠA族称为碱金属元素(氢除外); ⅡA族称为碱土金属元素; ⅢA族称为铝族元素; ⅣA族称为碳族元素; ⅤA族称为氮族元素; ⅥA族称为氧族元素; ⅦA族称为卤族元素。 元素周期表共有七个横行,称为七个周期, 其中第一(2种元素) 二(8种元素)
三(8种元素)周期为短周期(只有主族元素) 第四(18种元素) 五(18种元素) 六(32种元素)周期为长周期(既有主族元素,又有过渡元素); 第七周期(目前已排26种元素)为不完全周期。 在元素周期表中,越在左下部的元素,其金属性越强;越在右上 部的元素(惰性气体除外),其非金属性越强。金属性最强的稳定性 元素是铯,非金属性最强的元素是氟。 在元素周期表中位于金属与非金属分界处的金属元素,其氧化物或氢氧化物通常具有两性,如Be、Al等。 主族元素的价电子是指其最外层电子;过渡元素的价电子是指其 最外层电子和次外层的部分电子;镧系、锕系元素的价电子是指其最 外层电子和倒数第三层的部分电子。 在目前的112种元素中,只有二十二种非金属元素(包括6种稀 有气体元素),其余九十种都是金属元素;过渡元素全部是金属元素。 在元素周期表中,位置靠近的元素性质相近。通常在周期表的右上部的元素用于合成新农药;金属与非金属分界处的元素用于制造半 导体材料;过渡元素用于制造催化剂和耐高温、耐腐蚀的合金材料等等。 从原子序数为104号往后的元素,其原子序数的个位数与其所在的副族序数、Ⅷ族(包括108、109、110三号元素)、主族序数分别 相等。第七周期若排满,最后0族元素的原子序数为118号。 同周期第ⅡA族和第ⅢA族元素的原子序数之差可能为1(第二、 三两周期)或11(第四、五两周期)或25(第六周期)。 若主族元素xA所在的第n周期有a种元素,同主族的yB元素所在的第n+1周期有b种元素,当xA、yB位于第IA族、ⅡA族时, 则有:y=x+a;当xA、yB位于第ⅢA~ⅦA族时,则有:y=x+b。
元素周期表测试题
第四节元素周期表 Ⅰ学习重点 1.掌握元素周期表的结构以及周期、族等概念. 2.掌握同主族、同周期元素性质的递变规律,并能运用原子结构知识解释这些递变规律. 3.学会运用周期表,掌握原子结构、元素性质和位置三者间的关系. 4.初步掌握两性氧化物、氢氧化物的概念. 5.了解元素周期律的发展史,理解周期表的意义. Ⅱ学习难点 1.同周期,同主族元素性质的递变规律. 2.结构、性质、位置的相互关系. 3.元素周期表的意义. 一、选择题 1.某元素X,它的原子最外层电子数是次外层电子数的2倍,则X在周期表中位于( ) A.第二周期 B.第三周期 C.ⅣA族 D.ⅤA族 2.具有下列特征的元素,一定是主族元素的是( ) A.原子序数为86 B.最外层只有2个电子 C.次外层排满18个电子 D.最外层有4个电子 3.下列说法正确的是( ) A.非金属元素都是主族元素 B.主族元素的次外层电子数都是8 C.稀有气体元素都是主族元素 D.主族元素都是短周期元素 、Y、Z三种元素在周期表中,X、Y同主族,Y和Z同周期,它们的原子的最外层电子数之和为16,则这三种元素可能是( ) 、K、Ca 、P、S 、Cl、S 、S、Cl 5.下列说法中正确的是( ) A.周期表是按原子量逐渐增大的顺序从左到右排列的 B.最外层电子数相同的元素都是同一族 C.同族元素的最外层电子数一定相同 D.同周期元素的电子层数相同 6.与第二周期稀有气体元素的原子具有相同电子数的微粒是( ) + ++ 7.短周期元素X、Y可形成化合物X2Y3,若已知Y的原子序数为m,则X的原子序数不可能是( ) +5 +6 8.某元素R的原子核外电子数等于核内中子数,该元素单质与氧气充分反应可生成13g化合物RO,则该元素位于周期表中( ) A.第二周期 B.第三周期 C.ⅤA族 D.ⅡA族 9.原子序数为83的元素处于:①第五周期;②第六周期;③ⅣA族;④ⅤA族;⑤ⅡB族,其中正确的组合是( ) A①④ B.②③ C.②④ D.①⑤ 10.除一、二、三周期外,主族元素的次外层上( ) A.都是8个电子 B.都是18个电子 C.有的是8个电子,有的是18个电子 D.可以有8至18个电子 11.ⅠA、ⅡA、ⅢA主族金属元素的原子失去电子后,生成的阳离子的电子层结构
化学元素周期表知识整理
1 原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小; (2)同一族的元素从上到下,随电子层数增多,原子半径增大。 2 元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到 +7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同 (3) 所有单质都显零价 3 单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 4 元素的金属性与非金属性 (1)同一周期的元素电子层数相同。因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增; (2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。 5 最高价氧化物和水化物的酸碱性 元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。 6 非金属气态氢化物 元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。 7 单质的氧化性、还原性 一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。 [编辑本段]推断元素位置的规律 判断元素在周期表中位置应牢记的规律: (1)元素周期数等于核外电子层数; (2)主族元素的序数等于最外层电子数。
元素周期表测试题
第四节元素周期表 I学习重点 1. 掌握元素周期表的结构以及周期、族等概念 2. 掌握同主族、同周期元素性质的递变规律,并能运用原子结构知识解释这些递变规律? 3. 学会运用周期表,掌握原子结构、元素性质和位置三者间的关系 4. 初步掌握两性氧化物、氢氧化物的概念. 5. 了解元素周期律的发展史,理解周期表的意义 n学习难点 1. 同周期,同主族元素性质的递变规律. 2. 结构、性质、位置的相互关系. 3. 元素周期表的意义. 一、选择题 1. 某元素X,它的原子最外层电子数是次外层电子数的2倍,则X在周期表中位于() A. 第二周期 B. 第三周期 C. IV A族 D. V A族 2. 具有下列特征的元素,一定是主族元素的是() A. 原子序数为86 B. 最外层只有2个电子 C.次外层排满18个电子 D.最外层有4个电子 3. 下列说法正确的是() A. 非金属元素都是主族元素 B. 主族元素的次外层电子数都是8 C.稀有气体元素都是主族元素 D. 主族元素都是短周期元素 4. X、Y、Z三种元素在周期表中,X、Y同主族,Y和Z同周期,它们的原子的最外层电子数之和为16,则这三种元素可能是() A. Na、K、Ca B.N 、P、S C.F 、Cl、S D.O 、S、Cl 5. 下列说法中正确的是() A. 周期表是按原子量逐渐增大的顺序从左到右排列的 B. 最外层电子数相同的元素都是同一族 C. 同族元素的最外层电子数一定相同 D. 同周期元素的电子层数相同 6. 与第二周期稀有气体元素的原子具有相同电子数的微粒是() A. S2- B.NH 4+ C.Al3+ D.K+ 7. 短周期元素X、Y可形成化合物XzW,若已知Y的原子序数为m则X的原子序数不可能是() A. m+5 B.m-13 C.m+6 D.m-3 8. 某元素R的原子核外电子数等于核内中子数,该元素单质7.8g与氧气充分反应可生成13g 化合物RO则该元素位于周期表中() A. 第二周期 B. 第三周期 C. V A族 D. n A族 9. 原子序数为83的元素处于:①第五周期;②第六周期;③V A族;④V A族;⑤n B族,其中正确的组合是() A①④ B. ②③ C. ②④ D. ①⑤ 10. 除一、二、三周期外,主族元素的次外层上() A. 都是8个电子 B. 都是18个电子
元素周期表知识点总结(终极版)
元素周期表的高中化学问题终极总结 一、最外层电子数规律 1.最外层电子数为1的元素: 主族(IA族)、副族(I B、VIII族部分等)。 2.最外层电子数为2的元素: 主族(IIA族)、副族(II B、III B、IV B、VIIB族)、0族(He)、VIII族(26Fe、27Co等)。 3.最外层电子数在3~7之间的元素一定是主族元素。 4.最外层电子数为8的元素:0族(He除外)。 二、数目规律 1.元素种类最多的是第IIIB族(32种)。 2.同周期第IIA族与第IIIA族元素的原子序数之差有以下三种情况:(1)第 2、"3周期(短周期)相差1; (2)第 4、"5周期相差11; (3)第 6、"7周期相差
25。" 3.设n为周期序数,每一周期排布元素的数目为: 奇数周期为;偶数周期为。如第3周期为种,第4周期为种。 4.同主族相邻元素的原子序数: 第I A、IIA族,下一周期元素的原子序数=上一周期元素的原子序数+上一周期元素的数目;第IIIA~VIIA族,下一周期元素的原子序数=上一周期元素的原子序数+下一周期元素的数目。 三、化合价规律 1.同周期元素主要化合价: 最高正价由+1+7(稀有气体为0价)递变、最低负价由-4-1递变。 2.关系式: (1)最高正化合价+|最低负化合价|=8; (2)最高正化合价=主族族序数=最外层电子数=主族价电子数。 3.除第VIII族元素外,原子序数为奇(偶)数的元素,元素所在族的序数及主要化合价也为奇(偶)数。 四、对角线规律 金属与非金属分界线对角(左上角与右下角)的两主族元素性质相似,主要表现在第 2、"3周期(如Li和Mg、Be和Al、B和Si)。 五、分界线规律
元素周期表38个知识点归纳
人教版化学必修2第一章第一节元素周期表38个知识点归纳1、元素定义:核电荷数相同的同一类原子的总称,一种元素可能有多种形式的原子存在 形式,如:氢元素的几种形式:H、D(2 1H)、T(3 1 H)、H+、H-。 2、元素符号:在元素周期表中每个小格分四层,元素符号在第一层,黑色字体,用拉丁文大写字母表示,当大写字母相同时,加一个小写字母予以区别。 例如:H(氢)、He(氦);C(碳)、Cl(氯)、Ca(钙);N(氮)、Ne(氖)、Na (钠);Al(铝)、Ar(氩)。 3、元素名称:在元素周期表中每个小格分四层,元素名称在第二层,黑色字体,大多数元素的名称是由形声字构成,气态非金属的名称有气字头,固态非金属的名称有石头旁,液态非金属用三点水旁(溴),液态金属用水字底(汞),金属的名称都有金字旁,个别的元素的名称不是形声字,例如:氮不读“炎”音。 4、元素分类: (1)按元素所在的周期分类:同周期元素和不同周期元素 同周期元素共同点:电子层数相同,在元素周期表中处于同一行中,处于左右关系。 不同周期元素不同点:电子层数不相同,在元素周期表中不处于同一行中。 (2)根据元素的原子序数分类:前20号元素或第n号元素 (3)按元素所在的族分类:主族元素、副族元素、第VIII族元素、0族元素 (4)按元素周期表(新课标人教版化学必修2)分类:金属、非金属、过渡元素 其中金属元素专指主族元素的金属元素,非金属包括主族非金属和稀有气体,过渡元素是指所有副族金属元素和Ⅷ族金属元素,。 5、元素的特有数值:元素的原子序数和元素的相对原子质量。 (1)原子序数=核电荷数=质子数,原子序数在核组成符号中处于元素符号的左下角位置,在元素周期表中每个小格内的第一层,位于元素符号的左下角,数字呈鲜红色。 (2)元素的相对原子质量就是按照元素各核素原子的相对原子质量所占的一定百分比计算出的平均值(见课本P10),元素的相对原子质量在元素周期表中每个小格内的第四层,通常保留有效数字4位,数字呈黑色。 6、元素周期表 (1)将化学元素依照某种特有数值从小到大顺序依次排成一行,并将化学性质相似的元素依照某种特有数值从小到大排成一列所形成的表格叫元素周期表。 (2)元素周期表中特有数值:原子序数和相对原子质量。 (3)门捷列夫的元素周期表依照的特有数值是相对原子质量,现行的元素周期表依照的特有数值是原子序数。 7、元素周期表的结构:由七行和十八列构成,其中每一行为一个周期,从左到右第8、9、10列合起来为VIII族,其余每一列为一族,所以元素周期表由7个周期和16个族构成。
元素周期表测试题
元素周期表测试题 1.核电荷数大于10的某短周期元素,其原子最外电子层所含有的电子数是次外层所含有的 电子数的一半,有关该元素的单质或化合物的描述不正确的是() A.该元素在第三周期第W A族 B ?该元素的单质在常温下性质稳定,不易与水反应 C.该元素的氧化物不与酸反应,可与强碱的水溶液反应 D .该元素在地壳中的含量大,居所有元素的第二位 2.通过14C标记的C60进行跟踪研究,医学界发现了一种C60的羧酸衍生物在特定的条件下可通过断裂DNA杀死艾滋病病毒。有关C60和14C的叙述正确的是() A . 12C60与14C60互为同位素 B.14C转变为12C的过程属于化学变化 C.12C与叱的原子中含有的中子数之比为 3 : 4 D .金刚石与C60具有相同的物理性质 3?据国外有关资料报道,在独居石(一种共生矿,化学成分为Ce、La、Nb等的磷酸盐)中, 查明有尚未命名的116、124、126号元素。试判断116号元素应位于周期表的() A .第六周期第W A族 B .第七周期第W A族 Y的最高正价为m,则X的最高正价一定为m C.第七周期第四A族 D .第八周期第W A族 4.下列各表中的数字代表的是元素的原子序数。表中数字所对应的元素与它们在周期表中 的位置相符的是( 5.某种元素A的核外电子数等于核内中子数,取该元素的单质 得6 g化合物AO2,元素A在周期表中的位置是( 2.8 g跟氧气充分反应,可 A .第二周期n A族 B .第三周期W A族 C.第二周期W A族 D .第三周期V A族 6.有X、Y两种元素,原子 序数小于等于20, X的原子半径小于 且X、Y原子的最外X(OH)n为强碱,则Y(OH)n也一定为强碱 H n XO m为强酸,则X的氢化物溶于水一定显酸性 C. X元素形成的单质是X2,则Y元素形成的单质一定是丫2 )
物质结构元素周期律单元测试题
第一章物质结构元素周期律单元检测试题 一、单项选择题 (本题包括20小题,每小题只有一个选项符合题意,1-10每个2分,11-20每个3分,共50分) 1.根据元素在周期表中的位置判断,下列元素中原子半径最小的是 A.氧 B.氟 C.碳 D.氮 2.X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为()A.HX B.H2X C.XH4 D. XH3 3.下列物质中,含有非极性共价键的是 A.N2 B.CO2 C.NaOH D.CH4 4.下列关于3 2 He的说法正确的是 A.3 2He原子核内含有2个中子 B.3 2 He原子核内含有3个质子 C.3 2He原子核外有3个电子 D.3 2 He和4 2 He是两种不同的核素 5.已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是 A.元素非金属性按X、Y、Z的顺序减弱 B.阴离子的还原性按X、Y、Z的顺序减弱 C.气态氢化物的稳定性按X、Y、Z的顺序增强 D.单质的氧化性按X、Y、Z的顺序增强 6.含硒(Se)的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是() A.非金属性比硫强 B.氢化物比HBr稳定 C.原子序数为34 D.最高价氧化物的水化物显碱性 7.元素周期表里金属元素和非金属元素分界线附近能找到 A.新制农药元素 B.制催化剂元素 C.制半导体元素 D.制耐高温合金元素 8.下列说法正确的是 A.形成离子键的阴阳离子间只存在静电吸引力 B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 C.第三周期非金属元素含氧酸的酸性从左到右依次增强 D.元素周期律是元素原子核外电子排布周期性变化的结果 9.下列说法正确的是 A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强 B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强 D.第三周期元素的离子半径从左到右逐渐减小
元素周期表知识点总结
第一章物质结构元素周期律 第一节元素周期表 知识回顾: 1、原子的结构: 肿f时示F 原子是由原子核和电子组成;原子核由质子和中子组成 原子的质量集中在原子核上,电子的质量很小,几乎可以忽略不计 一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,中子不带电,所以原子对外显中性 2、元素的定义:具有相同核电荷数(质子数)的一类原子的总称 一、元素周期表的结构 1、原子序数 原子序数=核电荷数=质子数=核外电子数 2、周期 按原子序数递增的顺序,把电子层数相同的元素自左向右排成横行,每行叫做一个周期。 元素周期表共有七个周期,从上到下依次命名为第一周期、第二周期等 各周期内的信息表
3、族 按电子层数递增的顺序,把不同横行中最外层电子数相同的元素由上而下排成纵行,每一个纵行称为一个族?共18行 元素周期表共有十八个纵行,除& 9、10三个纵行叫第毗族外,其余每个纵行各为一个族,它们又被划分为十六个族。 族分为主族和副族,主族用罗马数字加“ A”表示,如I A族;副族用罗马数字 加” B”来表示,如U B。0族和毗族则不加“ A”或“ B” 注意:① 1,2行对应为I A,n A;13---17行对应为川A---A ②3---7行对应为川B --- W B; 11,12行对应为I B,n B o ③8,9,10对应为忸 ④18行对应0族 二、元素的性质与原子结构 1、碱金属元素 知识回顾:Na的物理性质和化学性质 从上到下原子的电子层数在增加,原子半径逐渐增大,所以失电子的能力逐渐增强从上到下金属性逐渐增强(金属性包括 碱金属元素的化学性质 R+2H2O====2ROH+H 4Li+Q====2L2O 4Na+Q====2Na;O(缓慢氧化) Na+Q==A ===Na s O2 2 卤族元素的主要物理性质
元素周期律和元素周期表知识总结
元素周期律和元素周期表知识总结 考试大纲要求 1.理解原子的组成及同位素的概念。掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系。 2.以第1、2、3周期的元素为例,掌握核外电子排布规律。 3.掌握元素周期律的实质及元素周期表(长式)的结构(周期、族)。 4.以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以ⅠA族和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。 知识规律总结 一、原子结构 1.几个量的关系() 质量数(A)=质子数(Z)+中子数(N) 质子数=核电荷数=原子序数=原子的核外电子数 离子电荷数=质子数-核外电子数 2.同位素 (1)要点:同——质子数相同,异——中子数不同,微粒——原子。 (2)特点:同位素的化学性质几乎完全相同;自然界中稳定同位素的原子个数百分数不变。 注意:同种元素的同位素可组成不同的单质或化合物,如H2O和D2O是两种不同的物质。 3.相对原子质量 (1)原子的相对原子质量:以一个12C原子质量的1/12作为标准,其它原子的质量跟它相比较所得的数值。它是相对质量,单位为1,可忽略不写。 (2)元素的相对原子质量:是按该元素的各种同位素的原子百分比与其相对原子质量的乘积所得的平均值。元素周期表中的相对原子质量就是指元素的相对原子质量。 4.核外电子排布规律 (1)核外电子是由里向外,分层排布的。 (2)各电子层最多容纳的电子数为2n2个;最外层电子数不得超过8个,次外层电子数不得超过18个,倒数第三层电子数不得超过32个。 (3)以上几点互相联系。 核外电子排布规律是书写结构示意图的主要依据。 5.原子和离子结构示意图 注意:①要熟练地书写1~20号元素的原子和离子结构示意图。 ②要正确区分原子结构示意图和离子结构示意图(通过比较核内质子数和核外电子数)。 6.微粒半径大小比较规律 (1)同周期元素(稀有气体除外)的原子半径随原子核电荷数的递增逐渐减小。 (2)同主族元素的原子半径和离子半径随着原子核电荷数的递增逐渐增大。 (3)电子层结构相同的离子,核电荷数越大,则离子半径越小。 (4)同种元素的微粒半径:阳离子<原子<阴离子。 (5)稀有气体元素的原子半径大于同周期元素原子半径。 (6)电子层数多的阴离子半径一定大于电子层数少的阳离子半径,但电子层数多的阳离子半径不一定大于电子层数少的阴离子半径。 二、元素周期律和周期表 1.位、构、性三者关系
最新高一化学元素周期表测试题
元素周期表单元检测题 无锡智学堂教育备课组 一、选择题 1.据报载我国最近合成多种元素的新的同位素,其中一种是18572Hf(铪),它的中子数是( ) A.72 B.113 C.185 D.257 2.某元素在自然界里由两种同位素组成,其原子个数比为 2.44∶1.05,第一种同位素的原 子 核内有29个质子和34个中子,第二种同位素原子核中的中子数比第一种多2个,该元素的平均原子量是( ) A.64.00 B.63.60 C.65.00 D.63.00 3.X 、Y 、Z 代表三个不同的短周期元素.X 元素的原子最外层只有一个电子;Y 元素在周期表 中位于第三周期,与磷元素相邻;Z 原子的L 电子层有6个电子,由这三种元素组成化合物的化学式可能是 ( ) A.X 3YZ 4 B.X 4YZ 4 C.XYZ 2 D.X 2YZ 4 4.A 、B 、C 、D 、E 是同一周期的五种主族元素,A 和B 的最高价氧化物对应的水化物均呈碱性,且碱性B >A ,C 和D 的气态氢化物的稳定性C >D ;E 是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( A.A 、B 、C 、D 、 E B.E 、C 、D 、B 、A C.B 、A 、D 、C 、E D.C 、D 、A 、B 、E 5.科学家根据元素周期律和原子结构理论预测,原子序数为114的元素属于第七周期ⅣA 族, 称为类铅元素.下面关于它的原子结构和性质预测正确的是( ) A.类铅元素原子的最外层电子数为4 B.其常见价态为+2、+3、+4 C.它的金属性比铅强 D. 6.对于X —O —H 型化合物而言,X 是除H 、O 外的其他元素时,下列说法中正确的是( ) A.当X 是活泼金属时,它一定是强碱 B.当X 是非金属性很强的元素时,X —O —H 一定是强酸 C.X —O —H 的水溶液不能导电 D.X —O —H 一定是共价化合物 7.下列各组顺序的排列不正确的是( ) A.离子半径:Na +>Mg 2+>Al 3+>F B.热稳定性:HCl >H 2S >PH 3>AsH 3 C.酸性强弱:H 2AlO 3<H 2SiO 4<H 2CO 3<H 3PO 4 D.溶点:NaCl >SiO 2>Na >CO 2 8.某元素X 的最高价氧化物的分子式为X 2O 5,在它的气态氢化物中含氢3.85%,则该元素 的原子量为( ) A.14 B.31 C.74.9 D.121.8 9.下列分子中,属于含有极性键的非极性分子是( ) A.H 2O B.Cl 2 C.SiCl 4 D.CH 3Cl 10.某元素原子的质量数为A ,它的阴离子X n-核外有x 个电子,w 克这种元素的原子核内中子数为( ) A. mol w n x A A )(+- B .mol A n x A w )(-+ C .mol A n x A w )(+- D.mol A n x A w )(-- 11.某主族元素R 的最高正价与最低负化合价的代数和为4,由此可以判断( ) A.R 一定是第四周期元素 B.R 一定是ⅣA 族元素 C.R 的气态氢化物比同周期其他元素气态氢化物稳定 D.R 气态氢化物化学式为H 2R 12.下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的 位置相符的是 ( )
元素周期表知识大全
一、元素周期表的结构 (一)编排三原则: 1. 按原子序数递增顺序从左到右排列。 2. 将电子层数相同的元素排列成一个横行。 3. 把最外电子层的电子数相同的元素按电子层数递增的顺序由上而下排列成纵行。 (二)周期:具有相同电子层数的元素按照原子序数递增的顺序排列的一行,叫周期。 (1)周期序数= 电子层数。周期序数用阿拉伯数字表示。 (2)元素周期表目前有7个周期。 第1、2、3周期称为短周期,分别含有2、8、8种元素;第4、5、6、7周期称为长周期,分别含有18、18、32、26种元素;第7周期又称为不完全周期。 (三)族 (1)元素周期表有18个纵行,称为族,共16个族。族序数用罗马数字表示。 (2)元素周期表中含有7个主族(ⅠA族~ⅦA族)、7个副族(ⅢB族~ⅦB族、ⅠB族~ⅡB族)、1个第Ⅷ族(三个纵行)和1个0族(稀有气体)。 (3)主族元素族序数= 最外层电子数。 (4)稀有气体元素化学性质不活泼,很难与其他物质发生化学反应,把它们的化合价定为0,因而叫做0族。 二、元素的性质与元素在周期表中位置的关系 (一)元素的金属性和非金属性与元素在周期表中位置 1、同周期从左到右,元素的金属性减弱,非金属性增强。 2、同主族从上至下,元素的金属性增强,非金属性减弱。 3、 (1 (2 域; (3 1 2、主族元素化合价的判断。 (1)元素最高正化合价的数值=族的序数=最外电子层电子数(即价电子数) (2)非金属元素最低负化合价的绝对值=8-其最高正化合价
三、元素周期律和元素周期表的意义 1869年,门捷列夫发现了元素周期律,并编制了第一张元素周期表。元素周期表是学习研究的一种重要工具。门捷列夫用元素周期律预言了未知元素,为发现新元素提供了线索。元素周期律与元素周期表可以指导工农业生产。 【典型例题】 [例1] 对比下列两组元素性质: (1)下列各组元素最高价氧化物对应的水化物碱性逐渐减弱、酸性逐渐加强的是( ) A. NaOH 、2)(OH Mg 、43PO H 、42SO H B. KOH 、NaOH 、42SO H 、4HClO C. 2)(OH Ca 、2)(OH Ba 、4HBrO 、4HClO D. 2)(OH Mg 、2)(OH Ba 、43PO H 、42SO H (2)下列各组气态氢化物稳定性由强到弱的顺序正确的是( ) A. 4SiH 、3PH 、S H 2、HCl B. HF 、HCl 、HBr 、HI C. 3PH 、S H 2HCl 、HF D. 3NH 、3PH 、3AsH 、HF 精析: (1)A 项第三周期的Na 、Mg 、P 、S 四元素最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强。B 项钾、钠是同主族,钾在钠的下方,则KOH 的碱性大于NaOH 的碱性。钠、硫、氯又是同一周期元素且按原子序数增加顺序排列的,由同周期元素组成最高价氧化物的水化物的碱性逐渐减弱,酸性逐渐增强的规律,推断出NaOH 、42SO H 、4HClO 符合此规律。C 项2)(OH Ca 与2)(OH Ba 的碱性22)()(OH Ca OH Ba ,因同主族钡在钙下方,碱性强。不难推断C 项不符题意。D 项Mg 、Ba 同主族,钡在下面碱性强于2)(OH Mg 与C 项相似。 (2)是气态氢化物稳定性的对比,这就需要对比元素的非金属性强弱。先确立元素位置再根据递变规律进行推断。A 项硅、磷、硫、氯分别是14、15、16与17号元素且在同一周期,其非金属性逐渐加强,故其氢化物稳定性逐渐增强,不符合题意。B 项氟、氯、溴、碘是VIIA 族卤素且按原子序数递增顺序排列的。其气态氢化物稳定性由强到弱,符合题意。C 项磷、硫、氯是同周期按原子序数递增排列的,其非金属性逐渐增强,气态氢化物稳定性逐强。氯、氟同主族其气态氢化物稳定性也是逐渐加强,不符合题意。D 项氮、磷、砷是按原子序数递增排列的,同主族元素其气态氢化物稳定性逐渐减弱,符合题意。但氮、氟同周期,氟位于氮的右方,非金属性强,当然更强于磷、砷的非金属性,从整体看不符合题意。 答案:(1)A 、B (2)B
相关文档
- 元素周期表知识点总结(终极版)
- 第一章第一节元素周期表知识点归纳
- 元素周期表知识点总结(终极版)
- 知识讲解_元素周期表(基础)知识讲解
- 化学元素周期表知识点精选总结
- 精 高中化学元素周期表知识点详解
- 元素周期表知识点总结(终极版)汇编
- 元素周期表知识大全
- 元素周期表个知识点归纳
- 元素周期表知识点总结
- (完整word版)必修二元素周期表知识点
- 化学元素周期表知识整理
- 化学元素周期表知识整理
- 元素周期表知识点总结
- 高中化学元素周期表知识点详解
- 元素周期表知识点总结60729
- 化学元素周期表知识整理
- 元素周期表知识点总结
- (完整版)元素周期表知识点总结(终极版)
- 元素周期表知识点总结67037
